III. CHẤT DIỆN HOẠT
Chất diện hoạt là bộ phận cần thiết vô nghành nghề phát triển hóa mỹ phẩm, nhất là vô quan hệ đằm thắm hệ keo dán và mặt phẳng xúc tiếp, bọn chúng hoàn toàn có thể tương tác, hấp phụ lên mặt phẳng xúc tiếp và thực hiện rời đáng chú ý mức độ căng mặt phẳng. Chất diện hoạt có không ít phần mềm, bọn chúng hoàn toàn có thể được sử dụng để: nhũ hóa, hòa tan, thực hiện độ ẩm và tẩy cọ. Chất diện hoạt phong phú bên trên thị ngôi trường, tuy nhiên cơ phiên bản được phân thành 2 group dựa vào cấu trúc: đằm thắm nước và đằm thắm dầu. Chất diện hoạt đằm thắm nước hoàn toàn có thể được phân thành dạng ion hoặc ko ion, trong lúc group kị nước thông thường chứa chấp bộ phận hydrocarbon, fluorocarbon, silicone.
1. HLB
Chất diện hoạt chứa chấp cả group đằm thắm nước và đằm thắm dầu vô công thức, nhằm review phần nào là trội rộng lớn, người tao nhờ vào chỉ số HLB. Tại tê liệt, HLB (hydrophilic-lipophilic balance) được gọi là chỉ số thăng bằng dầu-nước, hoàn toàn có thể kể từ 0 cho tới 40. HLB càng tốt thì hóa hóa học càng dễ dàng hòa tan nội địa, HLB càng thấp thì hóa hóa học càng dễ dàng hòa tan trong những dung môi đằm thắm dầu.
Bạn đang xem: hlb la gi
HLB hoàn toàn có thể được xem vị nhiều công thức không giống nhau. Griffin vẫn triển khai việc phân tích về những nhũ tương và đo lường chỉ số HLB mang lại từng hóa học diện hoạt. Một cách thức không giống được J. T. Davies đưa ra, ông tính HLB dựa vào số group đằm thắm dầu và đằm thắm nước bên trên 1 hóa học diện hoạt:
Trong đó: Chỉ số HLB = Tổng độ quý hiếm những group đằm thắm nước +
Tổng độ quý hiếm những group đằm thắm dầu + 7
Giá trị những group đằm thắm dầu – đằm thắm nước được liệt kê vô bảng sau:
| Nhóm | Giá trị nhóm | Nhóm | Giá trị nhóm |
| Nhóm đằm thắm nước:
-SO3Na -COOK -COONa N – amin bậc 4 Ester (vòng sorbital) Ester (-COOH, -OH, -O-, -OH) |
38,7
21,2 19,1 9,4 6,8 2,4 |
Thân dầu:
-CH- -CH2– -CH =CH- Nhóm khác -(CH2-CH2-O)- -(CH2-CH2-CH2-O)- |
-0,475
-0,475 -0,475 -0,475 0,33 -0,15 |
Ngoài đi ra, bám theo Kawakami thì chỉ số HLB hoàn toàn có thể được xem bám theo lượng của những group đằm thắm nước và đằm thắm dầu, công thức tính như sau:
Trong tê liệt, Mw là lượng của những group đằm thắm nước, còn Mo là lượng của tập thể nhóm đằm thắm dầu.
Kể kể từ Khi chỉ số HLB cho từng bộ phận được xem sẵn, việc đo lường HLB của hóa học nhũ hóa cần thiết nhằm nhũ mang lại láo lếu hợp ý bộ phận thuận tiện rộng lớn thật nhiều. Ví dụ tao sở hữu láo lếu hợp ý bao gồm 10% sáp ong (HLB 15), 53% Paraffin lỏng (HLB 10) và 37% petrolatum (HLB 10,5). Như vậy đòi hỏi HLB cần thiết muốn tạo nhũ tương dạng D/N được xem như sau:
Như vậy, nhằm nhũ hóa láo lếu hợp ý bên trên, tao cần thiết hóa học nhũ hóa sở hữu chỉ số HLB kể từ 10-11. Bảng sau đây cung ứng vấn đề về chỉ số HLB mang lại một số trong những nguyên vật liệu thô.
| Nguyên liệu thô | Nhũ tương N/D | Nhũ tương D/N |
| Các hydrocarbon
Paraffin lỏng (nhẹ) Paraffin lỏng (nặng) Vasiline (trắng) Sáp vi tinh anh thể Paraffin (rắn) Dầu, mỡ, sáp động thực vật Cotton seed oil Candelilla wax Carnauba wax Beeswax Lanolin (anhydrous) Xem thêm: quân thiếu cưng chiều cô vợ thiên hậu Acid, alcol Khủng khác Acid stearic Cetyl alcohol Silicone oil (G.E.) |
4
4 4 – 4 – – – 5 8 – – – |
10
10,5 10,5 9,5 9 7,5 14,5 14,5 10-16 15 17 13 10,5 |
Chỉ số HLB đặc biệt hiệu suất cao và thuận tiện trong công việc xác lập đặc thù của hóa học diện hoạt. Mối tương quan đằm thắm chỉ số HLB và phần mềm của hóa học diện hoạt được liệt kê bên dưới đây:
| HLB | Ứng dụng chính |
| 1,5-3
4-6 7-9 8-18 13-15 15-18 |
Chống tạo ra bọt
Nhũ tương Nước/Dầu Giữ ẩm Nhũ tương Dầu/Nước Chất tẩy Hòa tan |
Trong quy trình phân tích, Shinoda nhận ra rằng, chỉ số HLB của những hóa học diện hoạt ko ion thay cho thay đổi bám theo sức nóng chừng, kể từ tê liệt ông khuyến cáo một khá niệm tương quan, được gọi là sức nóng chừng HLB. Nhiệt chừng HLB là nấc sức nóng nhưng mà ở tê liệt, tính đằm thắm nước và đằm thắm dầu của hóa học diện hoạt được thăng bằng. Tại nấc sức nóng thấp rộng lớn sức nóng chừng HLB, nhũ tương D/N được tạo hình, còn ở tầm mức sức nóng cao hơn nữa sức nóng chừng HLB, tạo hình nhũ tương N/D.
2. Sự tạo hình Micell
Khi ở mật độ loãng, hỗn hợp những hóa học diện hoạt sở hữu tình hóa học tương tự động giống như các hỗn hợp thường thì, song Khi tăng chậm rãi dần dần cho tới mật độ chắc chắn, những phân tử hóa học diện hoạt này chính thức kết tụ lại cùng nhau, tạo ra trở thành hình cầu, trụ hoặc màng với quánh điểm: phần vỏ đằm thắm nước và phần lõi đằm thắm dầu vô môi trường xung quanh đằm thắm nước, và ngược lại phần vỏ đằm thắm dầu, lỗi đằm thắm nước vô môi trường xung quanh đằm thắm dầu. Sự tạo hình micell na ná độ dài rộng, con số của bọn chúng tiếp tục tùy thuộc vào chỉ số thăng bằng đằm thắm dầu – đằm thắm nước (HLB) và đặc thù từng loại hóa học diện hoạt.
Xem thêm: bé con còn nhỏ
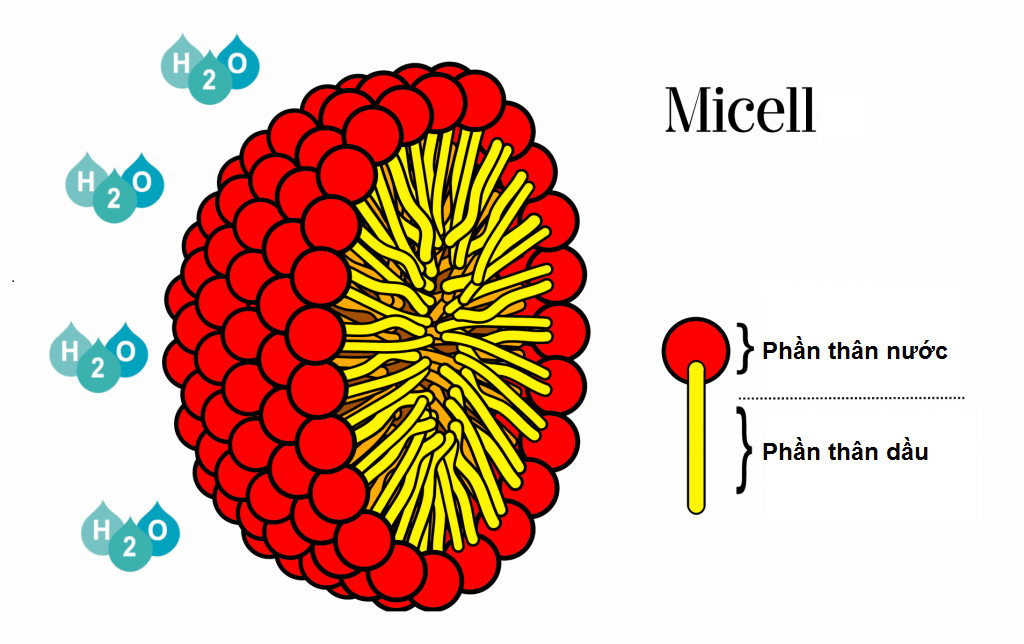 |
| Cấu trúc phân tử micell |
Mức mật độ của hóa học diện hoạt bên trên thời khắc tạo hình micell gọi là mật độ micell cho tới hạn (CMC), ranh giới này tạo ra nhiều sự thay cho thay đổi về đặc điểm lý hóa của hệ như thể hóa học (dung dịch lịch sự dạng keo), mức độ căng mặt phẳng, áp suất thấm vào, sức nóng chừng sầm uất đặc…
Nồng chừng micell cho tới hạn (CMC) hoàn toàn có thể xác lập bằng phương pháp thay cho thay đổi mật độ của hóa học diện hoạt, cho tới Khi tạo ra sự thay cho thay đổi về thể hóa học của hệ. CMC được xác lập vị sức khỏe vô cùng của những group đằm thắm dầu và đằm thắm nước.
Trong thực tiễn, những hóa học cơ học thông thường ko tan nội địa tuy nhiên lại hòa tan trong những micell của những hóa học diện hoạt được gọi là việc hòa tan hóa. Như vậy, hóa học diện hoạt được xem như thể hóa học trung gian trá hòa tan trong số những hóa học cơ học (thân dầu) và dung môi đằm thắm nước. Sự hòa tan này tùy thuộc vào con số và độ dài rộng những micell, con số đa dạng thì chừng hòa tan càng chất lượng, độ dài rộng micell càng rộng lớn thì những hóa học cơ học hòa tan càng đơn giản và dễ dàng.











Bình luận